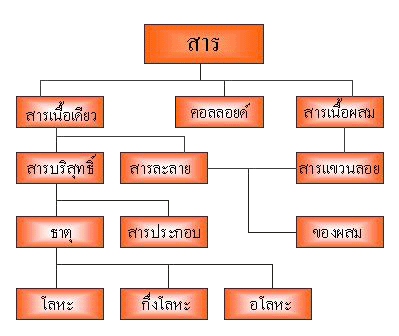
สสารและการจำแนก
สาร และ สมบัติของสาร
สสาร ( Matter ) หมายถึงสิ่งที่มีมวล ต้องการที่อยู่ และ
สามารถสัมผัสได้โดยประสาทสัมผัสทั้ง 5 เช่น ดิน น้ำ อากาศ ฯลฯ
ภายใน สสารเป็นเนื้อของสสาร เรียกว่า สาร (
Substance )
สาร ( Substance ) คือ สสารที่ทราบสมบัติ หรือ
สสารที่จะศึกษา ดังนั้นจึงเป็นสสารที่เฉพาะเจาะจง
ซึ่งจะมีสมบัติของสาร
2 ประเภท คือ
- สมบัติกายภาพ ( Physical Property ) หมายถึง
สมบัติที่สังเกตได้จากลักษณะภายนอก และ เกี่ยวกับวิธีการทางฟิสิกส์ เช่น
ความหนาแน่น , จุดเดือด ,
จุดหลอมเหลว
- สมบัติทางเคมี ( Chemistry Property ) หมายถึง
สมบัติที่เกิดขึ้นจากการทำปฏิกิริยาเคมี เช่น การติดไฟ , การเป็นสนิม ,
ความเป็น กรด - เบส
ของสาร
การเปลี่ยนแปลงสาร
การเปลี่ยนแปลงสาร
แบ่งออกเป็น 2 รูปแบบ คือ
- การเปลี่ยนแปลงทางกายภาพ (
Physical Change ) หมายถึง
การเปลี่ยนแปลงของสารที่เกี่ยวกับสมบัติกายภาพ
โดยไม่มีผลต่อ องค์ประกอบภายใน และ
ไม่เกิดสารใหม่ เช่น การเปลี่ยนสถานะ , การละลายน้ำ
- การเปลี่ยนแปลงทางทางเคมี ( Chemistry Change ) หมายถึง
การเปลี่ยนแปลงของสารที่เกี่ยวข้องกับสมบัติทางเคมีซึ่งมีผลต่อองค์ประกอบภายใน
และจะมีสมบัติต่างไปจากเดิม นั่นคือ การเกิดสารใหม่ เช่น กรดเกลือ ( HCl )
ทำปฏิกิริยากับลวด แมกนีเซียม ( Mg )
แล้วเกิดสารใหม่ คือ ก๊าซไฮโดรเจน ( H2 )
การจัดจำแนกสาร
จะสามารถจำแนกออกเป็น
4 กรณี
ได้แก่
1. การใช้สถานะเป็นเกณฑ์ แบ่งออกเป็น 3 กลุ่ม คือ
-
สถานะที่เป็นของแข็ง ( Solid ) จะมีรูปร่าง และ ปริมาตรคงที่
ซึ่งอนุภาคภายในจะอยู่ชิดติดกัน เช่น ด่างทับทิม ( KMnO4 ) ,
ทองแดง ( Cu )
-
สถานะที่เป็นของเหลว ( Liquid ) จะมีรูปร่างตามภาชนะที่บรรจุ และ มีปริมาตรที่คงที่
ซึ่งอนุภาคภายในจะอยู่ชิดกันน้อยกว่าของแข็ง และ
มีสมบัติเป็นของไหล เช่น น้ำมัน , แอลกอฮอล์ , ปรอท ( Hg ) ฯลฯ
-
สถานะที่เป็นก๊าซ ( Gas ) จะมีรูปร่าง และ ปริมาตรที่ไม่คงที่ โดยรูปร่าง
จะเปลี่ยนไปตามภาชนะที่บรรจุ อนุภาคภายในจะอยู่ ห่างกันมากที่สุด และ มีสมบัติเป็นของไหลได้
เช่น ก๊าซหุงต้ม ,
อากาศ
2. การใช้เนื้อสารเป็นเกณฑ์
จะมีสมบัติทางกายภาพของสารที่ได้จากการสังเกตลักษณะความแตกต่างของเนื้อสาร
ซึ่งจะจำแนกได้ออกเป็น 2 กลุ่ม คือ
- สารเนื้อเดียว ( Homogeneous
Substance ) หมายถึง
สารที่มีเนื้อสารเหมือนกันทุกส่วน
ทำให้สารมีสมบัติเหมือนกันตลอดทุกส่วน เช่น
แอลกอฮอล์ , ทองคำ ( Au ) , โลหะบัดกรี
- สารเนื้อผสม ( Heterogeneous
Substance ) หมายถึง
สารที่มีเนื้อสารแตกต่างกันในแต่ละส่วน จะทำให้สารนั้นมีสมบัติ
ไม่เหมือนกันตลอดทุกส่วน เช่น น้ำอบไทย ,
น้ำคลอง
ฯลฯ
3.
การละลายน้ำเป็นเกณฑ์
จะจำแนกได้ออกเป็น 3 กลุ่ม คือ
-
สารที่ละลายน้ำได้ เช่น เกลือแกง ( NaCl ) , ด่างทับทิม ( KMnO4 ) ฯลฯ
-
สารที่ละลายน้ำได้บ้าง เช่น ก๊าซคลอรีน ( Cl2 ) , ก๊าซคาร์บอนไดออกไซด์ ( CO2 ) ฯลฯ
-
สารที่ไม่สามารถละลายน้ำได้ เช่น กำมะถัน ( S8 ) , เหล็ก ( Fe ) ฯลฯ
4. การนำไฟฟ้าเป็นเกณฑ์
จะจำแนกได้ออกเป็น
2 กลุ่ม ได้แก่
-
สารที่นำไฟฟ้าได้ เช่น ทองแดง ( Cu ) , น้ำเกลือ
ฯลฯ
-
สารที่ไม่นำไฟฟ้า เช่น หินปูน ( CaCO3 ) ,
ก๊าซออกซิเจน ( O2
)
แต่โดยส่วนใหญ่นักเคมี
จะแบ่งสารตามลักษณะเนื้อสารเป็นเกณฑ์ ดังนี้

สารบริสุทธิ์ ( Pure Substance
) คือ
สารเนื้อเดียวที่มีจุดเดือด และ
จุดหลอมเหลวคงที่
ธาตุ ( Element ) คือ
สารบริสุทธิ์ที่ประกอบด้วยอะตอมเพียงชนิดเดียวกัน เช่น คาร์บอน ( C ) , กำมะถัน (
S8 )
สารประกอบ ( Compound Substance ) เกิดจากธาตุตั้งแต่ 2 ชนิดขึ้นไปมารวมกัน
โดยมีอัตราส่วนในการร่วมกันคงที่แน่นอนได้แก่
กรดน้ำส้ม ( CH3COOH ) ,
กรดไฮโดรคลอริก ( HCl )
ฯลฯ
ของผสม ( Mixture ) หมายถึง สารที่เกิดจากการนำสารตั้งแต่ 2
ชนิดขึ้นไปมาผสมกันโดยไม่จำกัดส่วนผสม และ
ในการผสมกัน
นั้นไม่มีปฏิกิริยาเกิดขึ้นระหว่างสารองค์ประกอบที่นำมาผสมกัน
ซึ่งมี 3 ประเภท ได้แก่
1. สารละลาย ( Solution Substance
)
เป็นสารเนื้อเดียวที่มีสัดส่วนในการรวมกันของธาตุ หรือ
สารประกอบไม่คงที่ไม่สามารถเขียนสูตรได้อย่างแน่นอน
และ มีขนาดอนุภาคที่เล็กกว่า 10-7 เซนติเมตร ซึ่งมี 3 สถานะ เช่น อากาศ , น้ำอัดลม , นาก , และ
โลหะผสม ทุกชนิด ฯลฯ
ซึ่งสารละลายจะแบ่งออกเป็น 2 ส่วน ได้แก่ ตัวทำละลาย ( Solvent ) และ ตัวถูกละลาย (
Solute ) จะมีข้อสังเกต ดังนี้
- สารใดที่มีปริมาณมากจะเป็นตัวทำละลาย และ
สารใดมีปริมาณน้อยจะเป็นตัวถูกละลาย เช่น
แอลกอฮอล์ฆ่าเชื้อ มีเอทานอล 70 % และ น้ำ
( H2O ) 30 % หมายความว่า
น้ำจะเป็นตัวถูกละลาย และ เอทานอลเป็นสารละลาย
เพราะแอลกอฮอล์มีปริมาณตามเปอร์เซนต์ที่มากกว่าน้ำ
- สารใดที่มีสถานะเช่นเดียวกับสารละลายเป็นตัวทำละลาย
เช่น
น้ำเชื่อม
ซึ่งน้ำเชื่อมจัดอยู่ในสภาพที่เป็นของเหลว ( Liquid ) ดังนั้นจึงสรุปได้ว่า
น้ำเป็นตัวทำละลาย และ น้ำตาลทราย ( C12H22O11 )
เป็นตัวถูกละลาย
2. สารแขวนลอย ( Suspension Substance
) คือ
สารที่เกิดจากอนุภาคขนาดเส้นผ่าศูนย์กลางที่มากกว่า 10-4 เซนติเมตร
ซึ่งจะลอยกระจายอยู่ในตัวกลางโดยอนุภาคที่มีอยู่ในของผสมนั้นมีขนาดใหญ่
จึงสามารถมองเห็นอนุภาคในของผสมได้อย่างชัดเจน เมื่อตั้งทิ้งไว้ อนุภาคจะตกตะกอนลงมา
ซึ่งสารแขวนลอยนั้นจะไม่สามารถผ่านได้ทั้งกระดาษกรอง และ กระดาษเซลโลเฟน เช่น โคลน
, น้ำอบไทย
3. คอลลอยด์ ( Colliod ) จะประกอบด้วยอนุภาคขนาดเส้นผ่าศูนย์กลางระหว่าง 10-4 และ 10-7 เซนติเมตร ซึ่งจะไม่มีการตกตะกอน สามารถกระเจิงแสงได้ ซึ่งเรียกปรากฏการณ์นี้ว่า
" ปรากฏการณ์ทินดอลล์ " และ
ภายในอนุภาคก็มีการเคลื่อนที่แบบบราวน์เนียน(
Brownian Movement ) กล่าวคือ เป็นการเคลื่อนที่ที่ไม่แน่นอน ในแนวเส้นตรง
ซึ่งจะสามารถส่องดูได้จากเครื่องที่เรียกว่า "
อัลตราไมโครสโคป " ( Ultramicroscope ) ซึ่งคอลลอยด์จะสามารถผ่านกระดาษกรองได้
แต่ไม่สามารถผ่านกระดาษเซลโลเฟนได้ เช่น กาว ,
นมสด
คอลลอยด์ในชีวิตประจำวัน
คอลลอยด์มีหลายชนิด ดังนี้
|
ประเภทของคอลลอยด์ |
สถานะของอนุภาค |
สถานะของตัวกลาง |
ตัวอย่าง |
|
แอโรซอล |
ของเหลว |
ก๊าซ |
เมฆ , สเปรย์ , หมอก |
|
แอโรซอล |
ของแข็ง |
ก๊าซ |
ควันไฟ , ฝุ่น |
|
อิมัลชัน |
ของเหลว |
ของเหลว |
นมสด , น้ำกะทิ , สลัด |
|
เจล |
ของแข็ง |
ของเหลว |
เยลลี่ , วุ้น , กาว , ยาสีฟัน |
|
โฟม |
ก๊าซ |
ของเหลว |
ฟองสบู่ , ครีมโกนหนวด |
|
โฟม |
ก๊าซ |
ของแข็ง |
เม็ดโฟม , สบู่ก้อน |
คอลลอยด์ที่พบในชีวิตประจำวัน
คือ อิมัลชัน ( Emulsion ) โดยอิมัลชัน คือ คอลลอยด์ที่เกิดระหว่างของเหลว
กับของเหลว
ซึ่ง สามารถปนเป็นเนื้อเดียวกันได้โดยมีอิมัลซิฟายเออร์
( Emulsifier ) เป็นตัวประสาน เช่น
น้ำ + น้ำมัน (
ไม่สามารถรวมตัวกันได้ ) ดังนั้น
น้ำสบู่จึงเป็นอิมัลซิฟายเออร์เป็นตัวประสานจึงสามารถรวมตัวกันได้
การทดสอบความบริสุทธิ์ของสาร
มี 3 ประเภท ได้แก่
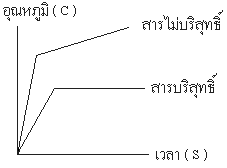
1. การหาจุดเดือด ( Boiling Point
) การที่สารไม่บริสุทธิ์
หรือ สารละลายจุดเดือดไม่คงที่
เกิดจากอัตราส่วนระหว่างจำนวนโมเลกุลของตัวถูกละลาย
และ ตัวทำละลาย
เปลี่ยนแปลงไปโมเลกุลที่มีจุดเดือดต่ำจะระเหยไปเร็วกว่าทำให้สารที่มีจุดเดือดสูงใน อัตราส่วนที่
มากกว่าจึงเป็นผลให้จุดเดือดสูงขึ้นเรื่อย ๆ
โดยดูจากรูปที่แสดงเป็นกราฟ
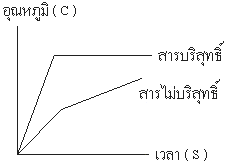
2. การหาจุดหลอมเหลว ( Melting Point
)
จะสามารถทดสอบกับสารที่บริสุทธิ์ และสารที่ไม่บริสุทธิ์ได้
โดย
- สารบริสุทธิ์จะมีจุดหลอมเหลวคงที่ และ
มีอุณหภูมิช่วงการหลอมเหลวแคบ
-
สารไม่บริสุทธิ์จะมีจุดหลอมเหลวไม่คงที่ และ
มีอุณหภูมิในช่วงการหลอมเหลวกว้างซึ่งอุณหภูมิฃ่วงการหลอม
หมายถึง อุณหภูมิที่สารเริ่มต้นหลอมจนกระทั่งสารนั้นหลอมหมดโดยในอุณหภูมิช่วงการหลอม ถ้าแคบต้องไม่เกิน
2 องศาเซลเซียส โดยดูจากรูปที่แสดงเป็นกราฟ
3. การหาจุดเยือกแข็ง ( Freezing Point
)
จะสามารถทดสอบกับสารบริสุทธิ์ และ สารไม่บริสุทธิ์ ซึ่งไม่ค่อยนิยม
เพราะจะต้อง ใช้เวลานานมากในการหาจุดเยือกแข็ง
โดย
- สารบริสุทธิ์จะมีจุดเยือกแข็งคงที่
- สารไม่บริสุทธิ์จะมีจุดเยือกแข็งไม่คงที่
โดยดูจากรูปที่แสดงเป็นกราฟ

การแยกสาร
ใช้ในการแยกสารประกอบซึ่งมี
7 วิธี ได้แก่
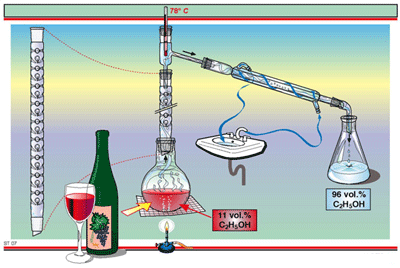
1. การกลั่น
เหมาะสำหรับแยกของเหลวที่ปนเป็นเนื้อเดียวกัน
โดยทำให้ของเหลวกลายเป็นไอ แล้วทำให้ควบแน่นเป็นของเหลวอีก
แบ่งออก เป็น 2 ประเภท
คือ
- การกลั่นธรรมดา เหมาะสำหรับสารที่มีจุดเดือดต่างกันประมาณ 80 องศาเซลเซียส ขึ้นไป
แต่อุณหภูมิตั้งแต่ 40 องศาเซลเซียส
ก็จะเกิดกระบวนการแล้ว
- การกลั่นลำดับส่วน เหมาะสำหรับสารที่มีจุดเดือดต่างกันเพียงเล็กน้อย ซึ่งจะมีข้อเสีย คือ จะใช้พลังงานเป็นจำนวนมาก และมีความสลับซับซ้อน การกลั่นลำดับส่วนบางครั้งไม่ได้แยกสารให้บริสุทธิ์ แต่แยกเพื่อประโยชน์ในการนำไปใช้ เช่น การแยกน้ำมันดิบ โดยจะแยกพวกที่มีจุดเดือดใกล้เคียงไว้ด้วยกัน แต่ถ้าสารที่มีจุดเดือดใกล้เคียงกันมาก แต่ไม่มีเครื่องกลั่นลำดับส่วนก็สามารถกลั่นได้ด้วยเครื่องกลั่นธรรมดา แต่จะต้องกลั่นหลาย ๆ ครั้ง จนกระทั่งจุดเดือด และจุดหลอมเหลวคงที่
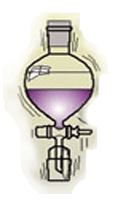
2. การใช้กรวยแยก
เหมาะสมกับสารที่เป็นของเหลว
และ จะต้องเป็นสารที่ไม่ละลายต่อกัน หรือ จะต้องมีขั้วต่างกัน เช่น น้ำ และ
น้ำมัน
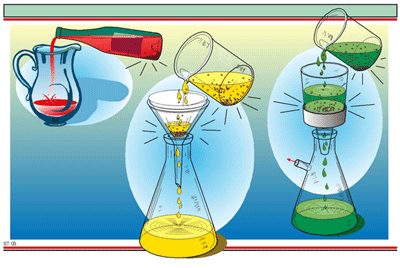
3. การกรอง
เหมาะสำหรับของแข็งที่ไม่ละลายน้ำ
หรือ ของแข็งที่ละลายน้ำ และ ไม่ละลายน้ำปนอยู่ด้วยกัน เช่น หินปูน และ น้ำ
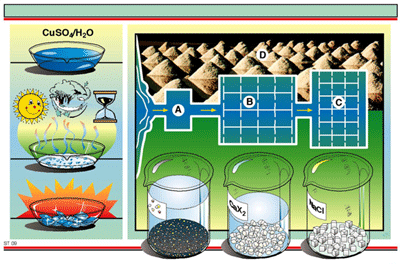
4. การตกผลึก
เหมาะสำหรับสารที่สามารถละลายได้เป็นปรากฏการณ์ที่ตัวถูกละลายที่เป็นของแข็ง
แยกตัวออกจากสารละลายได้เป็นของแข็งที่มีรูปทรงเรขาคณิต
โดยสารใด ๆ ที่ละลายในน้ำอยู่ในจุดอิ่มตัวจะตกเป็นผลึก
ถ้ามากเกินพอจะเป็นการตกตะกอนของสาร
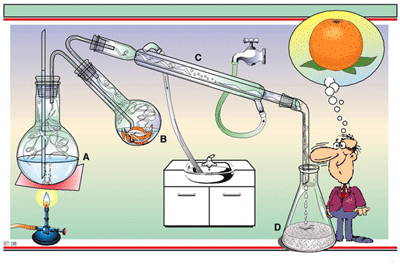
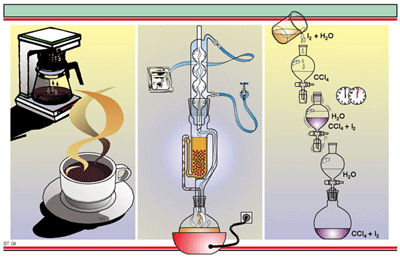
5. การสกัดด้วยไอน้ำ
เหมาะสมสำหรับการสกัดพวกน้ำมันหอมระเหยจากพืช
และ การทำน้ำหอม ( CH3COOH2O )
โดยมีหลักสำคัญ ดังนี้
-
จุดเดือดต่ำจะระเหยง่าย ถ้าเป็นสารที่มีจุดเดือดสูง
จะต้องการกลั่นโดยอาศัยการเปลี่ยนแปลงความดันในระบบ
-
สารส่วนใหญ่ไม่ละลายน้ำ
6. การสกัดด้วยตัวทำละลาย
เหมาะสมกับสารที่ระเหยง่าย
โดยมีหลักสำคัญดังนี้
-
ถ้าสารมีความสามารถในการละลายในตัวทำละลายต่างชนิดกันสามารถแยกสารออกจากกันได้
-
หลักการเลือกตัวทำละลายที่ดี คือ ต้องเลือกตัวทำละลายที่ดี คือ
ต้องเลือกตัวทำละลายที่ละลายสารที่ต่างกัน
การสกัดออกมามากที่สุด และสิ่งเจือปนนั้นจะต้องติดมาน้อยที่สุด
7. การโครมาโทรกราฟี
เหมาะสมสำหรับการแยกสารที่มความสามารถในการละลาย
และ ดูดซับไม่เท่ากัน , สารที่มีปริมาณน้อย และ ไม่มีสี โดยหลักสำคัญ
มีดังนี้
- ในการทดลองทุกครั้งจะต้องปิดฝา
เพื่อป้องกันตัวทำละลายแห้ง
ในขณะที่เคลื่อนที่บนตัวดูดซับ
-
ถ้าสารเคลื่อนทีใกล้เคียงกันมาก แสดงว่าสารมีความสามารถในการละลาย และ
ดูดซับได้ใกล้เคียง และ จะแก้ไขได้โดย
การเปลี่ยนตัวทำละลาย หรือ
เพิ่มความยาวของดูดซับได้ แต่สารที่เคลื่อนที่ได้ระยะทางเท่ากันในตัวทำละลาย และ
ตัวดูดซับใกล้เคียงกัน
มักจะสรุปได้ว่าสารนั้นเป็นสารเดียวกัน
โดยวิธีนี้สามารถทำให้สารบริสุทธิ์ได้
โดยตัดแบ่งสารที่ต้องการละลายในตัวทำละลายที่เหมาะสม แล้วระเหยตัวทำละลายนั้นทิ้งไป
แล้วนำสารนั้นมาทำการโครมาโทรกราฟีใหม่
จนได้สารบริสุทธิ์
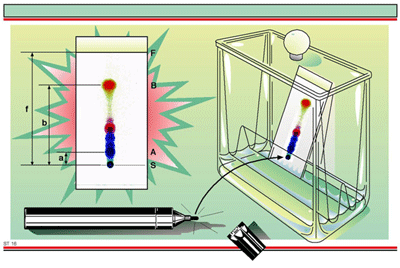
การคำนวณหาค่า Rf (
Rate of Flow ) เพื่อนำมาคำนวณค่าของสารละลาย
|
ค่า Rf = ระยะทางที่สารเคลื่อนที่ / ระยะทางที่ตัวทำละลายเคลื่อนที่ |
โดยค่า Rf ไม่มีหน่วย แต่มีค่าที่สูงสุดเท่ากับ 1