
อัตราการเกิดปฏิกิริยาเคมี
การเกิดปฏิกิริยาเคมี
การเกิดปฏิกิริยาเคมี
เป็นการเปลี่ยนแปลงของสารที่ได้ผลิตภัณฑ์ของสารที่แตกต่างจากสารเดิมโดยอาจสังเกตจากการเปลี่ยนสีของสาร
การเกิดตะกอน หรือการเกิดกลิ่นใหม่
ทฤษฎีที่ใช้อธิบายปฏิกิริยาเคมี มีอยู่ 2 ทฤษฎี คือ
1. ทฤษฎีการชน (The Collision Theory) ปฏิกิริยาเคมีจะเกิดขึ้นได้ ก็ต่อเมื่ออนุภาคของสารตั้งต้นต้องมาปะทะกันหรือมาชนกัน และการชนกันนั้นมีทั้งการชนที่ประสบผลสำเร็จ ดังภาพ

แบบจำลองการเกิดปฏิกิริยาเคมีตาม ทฤษฎีการ
2. ทฤษฎีแอกติเวเตดคอมเพลกซ์หรือทฤษฎีสภาวะทรานซิชัน (The Activated Complex Theory or The Transition State Theory) เป็นทฤษฎีที่ดัดแปลงมาจากทฤษฎีการชน โดยทฤษฎีนี้จะกล่าวถึงการชนอย่างมีประสิทธิภาพของสารตั้งต้นในลักษณะที่เหมาะสม โดยจะเกิดเป็นสารประกอบใหม่ชั่วคราว ที่เรียกว่า สารเชิงซ้อนกัมมันต์ (Activated Complex) ซึ่งในระหว่างการเกิดสารชนิดนี้พันธะเคมีของสารตั้งต้นจะอ่อนลง และเริ่มมีการสร้างพันธะใหม่ระหว่างคู่อะตอมที่เหมาะสม จนในที่สุดพันธะเก่าจะถูกทำลายลงอย่างสิ้นเชิง และจะมีพันธะใหม่ถูกสร้างขึ้นมาแทนที่ ดัง แบบจำลองการเกิดปฏิกิริยาเคมีต่อไปนี้

แบบจำลองการเกิดปฏิกิริยาเคมีตาม ทฤษฎีแอกติเวเตดคอมเพลกซ์
พลังงานกับการเกิดปฏิกิริยา
ในการเกิดปฏิกิริยาของสารแต่ละปฏิกิริยานั้น ต้องมีพลังงานเข้ามาเกี่ยวข้องกับการเกิดปฏิกิริยาเคมี 2 ขั้นตอน ดังนี้
ขั้นที่ 1
เป็นขั้นที่ดูดพลังงานเข้าไปเพื่อสลายพันธะในสารตั้งต้น
ขั้นที่ 2 เป็นขั้นที่คายพลังงานออกมาเมื่อมีการสร้างพันธะในผลิตภัณฑ์
ดังนั้นการเกิดปฏิกิริยาเคมีจะเกี่ยวข้องกับการเปลี่ยนแปลงพลังงาน ดังนี้
1. ปฏิกิริยาดูดความร้อน ( Endothermic reaction) เป็นปฏิกิริยาที่ดูดพลังงานเข้าไปสลายพันธะมากกว่าที่คายออกมาเพื่อสร้างพันธะ โดยในปฏิกิริยาดูดความร้อนนี้สารตั้งต้นจะมีพลังงานต่ำกว่าผลิตภัณฑ์ จึงทำให้สิ่งแวดล้อมเย็นลง อุณหภูมิลดลง เมื่อเอามือสัมผัสภาชนะจะรู้สึกเย็น ดังภาพ
2. ปฏิกิริยาคายความร้อน ( Exothermic reaction) เป็นปฏิกิริยาที่ดูดพลังงานเข้าไปสลายพันธะน้อยกว่าที่คายออกมาเพื่อสร้างพันธะ โดยในปฏิกิริยาคายความร้อนนี้สารตั้งต้นจะมีพลังงานสูงกว่าผลิตภัณฑ์ จึงให้พลังงานความร้อนออกมาสู่สิ่งแวดล้อม ทำให้อุณหภูมิสูงขึ้น เมื่อเอามือสัมผัสภาชนะจะรู้สึกร้อน ดังภาพ
 ............
............
แผนภูมิพลังงานของปฏิกิริยาดูดความร้อน .......แผนภูมิพลังงานของปฏิกิริยาคายความร้อน
อัตราการเกิดปฏิกิริยาเคมี
อัตราการเกิดปฏิกิริยาเคมี หมายถึง
ปริมาณสารตั้งต้นที่หายไปต่อหนึ่งหน่วยเวลา
หรือปริมาณผลิตภัณฑ์ที่เกิดขึ้นต่อหนึ่งหน่วยเวลา
เมื่อพิจารณาจากปฏิกิริยาต่อไปนี้
A + 2B -------------> C ..(1)
ในขณะที่ปฏิกิริยาดำเนินไป สาร A และสาร B เป็นสารตั้งต้นถูกใช้ไปดังนั้นความเข้มข้นของสาร A และ B จะลดลง ส่วนความเข้มข้นของสาร C ซึ่งเป็นผลิตภัณฑ์จะเพิ่มขึ้น จากปฏิกิริยา (1) จะพบว่าอัตราการลดลงของสาร A เป็นครึ่งหนึ่งของการลดลงของสาร B
ดังนั้นเมื่อเขียนความสัมพันธ์ระหว่างอัตราการเกิดปฏิกิริยาในรูปของสารต่างๆ จะต้องคิดต่อ 1 โมลของสารนั้น ซึ่งสามารถเขียนได้ดังนี้
อัตราการเกิดปฏิกิริยาเคมี = ปริมาณของสารตั้งต้นที่ลดลง/ เวลา
= ปริมาณของสารผลิตภัณฑ์ที่เกิดขึ้น / เวลา
อัตราเร็วเฉลี่ย หมายถึง อัตราเร็วโดยเฉลี่ย ตั้งแต่เริ่มต้น จนปฏิกิริยาเกิดขึ้นในช่วงเวลาหนึ่ง เช่น อัตราเร็วเฉลี่ยในช่วง 10 วินาที ( หาได้จากการทดลอง)
อัตราเร็ว ณ เวลาหนึ่ง หมายถึง อัตราเร็วของปฏิกิริยาที่ตำแหน่งใดตำแหน่งหนึ่ง เช่น อัตราเร็ว ณ 10 วินาที ( หาจากค่าความชันของกราฟระหว่างปริมาณสารกับเวลา)
ปัจจัยที่มีผลต่ออัตราการเกิดปฏิกิริยา
1. ความเข้มข้นของสารตั้งต้น กรณีที่สารตั้งต้นเป็นสารละลาย ถ้าสารตั้งต้นมีความเข้มข้นมากจะเกิดเร็ว เนื่องจากตัวถูกละลายมีโอกาสชนกันมากขึ้นบ่อยขึ้น ในทางตรงกันข้ามถ้าเราเพิ่มปริมาตรของสารละลายโดยความเข้มข้นเท่าเดิม อัตราการเกิดปฏิกิริยาจะเท่าเดิม

2. พื้นที่ผิวสัมผัส กรณีที่สารตั้งต้นมีสถานะเป็นของแข็ง สารที่มีพื้นที่ผิวสัมผัสมากจะทำปฏิกิริยาได้เร็วขึ้น เนื่องจากสัมผัสกันมากขึ้น ใช้พิจารณากรณีที่สารตั้งต้นมีสถานะของแข็ง ดังภาพ

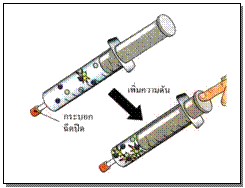
3. ความดัน กรณีที่สารตั้งต้นมีสถานะเป็นก๊าซ ถ้าความดันมากปริมาตรก็ลดลง และปฏิกิริยาก็จะเกิดได้เร็ว เนื่องจากอนุภาคของสารมีโอกาสชนกันมากขึ้นบ่อยขึ้นในพื้นที่ที่จำกัดนั่นเอง ดังภาพ
4. อุณหภูมิ การที่อุณหภูมิของสารตั้งต้นเพิ่มขึ้นอัตราการเกิดปฏิกิริยาจะเพิ่มขึ้น เนื่องจากเมื่ออุณหภูมิสูงขึ้น โมเลกุลของสารในระบบจะมีพลังงานจลน์สูงขึ้นและมีการชนกันของโมเลกุลมากขึ้น

ปฏิกิริยาที่อุณหภูมิต่ำ ปฏิกิริยาที่อุณหภูมิสูง
5. ตัวเร่งปฏิกิริยา (Catalyst) หมายถึงสารเคมีที่ช่วยทำให้อัตราการเกิดปฏิกิริยาเร็วขึ้นเนื่องจากตัวเร่งจะช่วยในการลดพลังงานกระตุ้นโดยช่วยปรับกลไกในการเกิดปฏิกิริยาให้เหมาะสมกว่าเดิม โดยจะเข้าไปช่วยตั้งแต่เริ่มปฏิกิริยาแต่เมื่อสิ้นสุดปฏิกิริยาจะกลับมาเป็นสารเดิม
6. ธรรมชาติของสาร เนื่องจากสารมีแรงยึดเหนี่ยวซึ่งแตกต่างกัน โดยปกติสารประกอบไอออนิกจะเคลื่อนที่ได้เร็วกว่าสารประกอบโควาเลนต์ ดังนั้นสารประกอบไอออนิกจะเกิดปฏิกิริยาเร็วกว่าสารประกอบโควาเลนต์